Roturas parciales del manguito rotador
Partial ruptures of the rotator cuff
Resumen:
El manguito rotador está formado por los músculos subescapular (anterior), supraespinosos e infraespinoso (manguito posterosuperior) y redondo menor (posterior), y su patología supone un motivo de consulta habitual. A nivel histológico, la inserción tendinosa se compone de 5 capas que se entremezclan hasta su unión con el hueso. Sin embargo, a nivel macroscópico estos tendones no son homogéneos, ya que existe una zona de debilidad en su inserción a nivel del trocánter mayor (zona crescent), donde se originan la mayoría de las roturas parciales del tendón. Existe también un engrosamiento conocido como “cable rotador” que permite la transmisión de fuerzas pese a que exista esta rotura. Además, en los últimos años ha ganado importancia el papel de la capa más articular, la cápsula, por lo que en la actualidad se considera que existe un complejo tendinocapsular.
El hallazgo radiológico de roturas parciales resulta muy frecuente y realizar una correcta interpretación diagnóstica que permita tomar las decisiones terapéuticas más adecuadas no siempre resulta sencillo. La progresión de estas roturas parciales suele requerir varios años y solo aquellos casos refractarios al tratamiento conservador precisarán cirugía.
El objetivo de este artículo es recoger trabajos destacados por su impacto o metodología que permiten entender la anatomía y la función del manguito posterosuperior, así como conocer la historia natural de la enfermedad y su correlación con la clínica, además de las principales opciones de tratamiento; solo entendiendo esta patología desde la base podremos diagnosticar y tomar las mejores decisiones para nuestros pacientes.
Abstract:
The rotator cuff is composed of the subscapularis (anterior), supraspinatus and infraspinatus (posterosuperior cuff) and teres minor (posterior) muscles, and damage to it is a common cause of consultation. Histologically, the tendon insertion consists of 5 layers that intermingle to their point of joining to the bone. However, macroscopically these tendons are not homogeneous, since there is a weak zone in their insertion at greater trochanter level (the crescent zone), where most of the tendon ruptures originate. There is also a thickening known as the "rotator cable", that allows force transmission despite the existence of such rupture. Moreover, in recent years the role of the most articular layer (the capsule) has gained importance; as a result, a tendon-capsule complex is now considered to exist.
The radiological finding of partial ruptures is very frequent, and a correct diagnostic interpretation allowing optimum therapeutic decision making is not always easy. The progression of such partial ruptures typically takes several years, and only those cases refractory to conservative management will need surgery.
The present article reviews studies of importance in view of their impact or methodology that allow us to understand the anatomy and function of the posterosuperior cuff, the natural history of the disorder and its correlation to the clinical manifestations, as well as the main treatment options. Only by understanding the fundaments of this kind of disorder can we diagnose and make the best decisions for our patients.
Introducción
Las lesiones del manguito rotador suponen una de las principales causas de consulta en la patología del hombro. Estas lesiones resultan difíciles de sistematizar e interpretar ya que, salvo en los pocos casos en los que existe un claro antecedente traumático, son lesiones progresivamente degenerativas de las partes blandas que solo en su estadio final acaban generando alteraciones óseas. Las roturas parciales del manguito (RPMR) se sitúan en esa “zona gris” de transición entre los tendones sanos y las roturas de espesor completo (RECMR); además, las lesiones radiológicas no son siempre patológicas(1), lo que hace más complejo su estudio y manejo. Esto, junto con la escasa literatura sobre roturas parciales en comparación con los estudios en RECMR, hace que exista aún mucha controversia al respecto. Una buena aproximación a esta patología podría ser el artículo de revisión publicado recientemente por la American Academy of Orthopaedic Surgeons (AAOS)(2).
El objetivo de este artículo es recoger trabajos destacados por su impacto o metodología que permiten entender la anatomía y la función del manguito posterosuperior, conocer la historia natural de la enfermedad y su correlación con la clínica, así como revisar las principales opciones de tratamiento que existen para realizar un adecuado diagnóstico y tomar las mejores decisiones para nuestros pacientes.
Entender la anatomía: Clark et al. (1992)(3)
En este exhaustivo trabajo de anatomía titulado “Tendons, ligaments and capsule of the rotator cuff. Gross and microscopic anatomy”, publicado en 1992, Clark y Harryman realizan una minuciosa descripción macro- y microscópica del manguito rotador. Estudiando 32 manguitos sanos en cadáver determinaron su configuración histológica en capas y describieron cómo estas se entrecruzan formando a su vez otras estructuras.
Este trabajo sienta las bases de las 5 capas histológicas del complejo tendinocapsular que sigue vigente hoy en día. Estas capas, de superficial a profunda, se disponen de la siguiente manera: la capa más superficial contiene arteriolas y está en continuidad con el ligamento coracohumeral (LCH); debajo se disponen haces fibrosos gruesos y ordenados; y, bajo estos, aparece una tercera capa de haces finos y desordenados. La cuarta capa la forma tejido conectivo laxo y bandas colágenas gruesas que se fusionan con el LCH en el borde más anterior del supraespinoso (SE); y, por último, en relación con la articulación, encontramos la cápsula glenohumeral con las fibras de Sharpey formando la unión con el hueso.
A nivel macroscópico los autores observaron que SE e infraespinoso (IE) se unen 1,5 cm antes de su inserción en el hueso. A esta inserción común se une, desde la zona posterior, el redondo menor (Rm), mientras que, en anterior, a través del techo y el suelo de la corredera, se entrecruzan con el subescapular (SbE). Este trabajo ya señala un engrosamiento visible en el lado capsular en forma de cuerda de arco al que posteriormente Burkhart dotaría de sentido funcional.
La anatomía es función: Burkhart et al. (1993)(4)
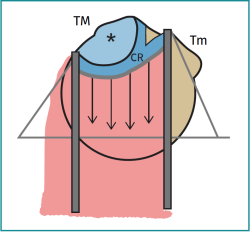
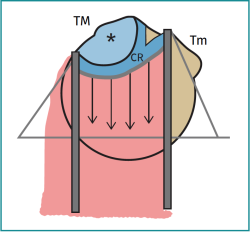
Este trabajo, titulado “The Rotator Crescent and Rotator Cable: An Anatomic Description of the Shoulder's ‘Suspension Bridge’”, publicado solo un año después, añade un concepto de anatomía funcional clave en el mecanismo de trabajo del manguito rotador, el conocido como “cable rotador”. Ya en 1931, Codman y Akerson describieron la “zona crítica” en la que comenzaban la mayoría de las roturas del manguito(5). Burkhart, como artroscopista, percibió que esta zona en media luna o zona crescent más débil estaba rodeada por un engrosamiento de la cápsula, como habían descrito Clark et al.(3). Tras diseccionar 20 cadáveres y realizar mediciones del grosor del tejido, encuentran que el cable tiene de media 2,55 veces el espesor de la zona crescent y, además, en los hombros de mayor edad, parece que el cable se va engrosando como respuesta adaptativa. De esta manera, Burkhart describe la estructura anatómica a través de la cual funciona su modelo biomecánico del manguito posterosuperior(6): el cable rotador trabaja como un puente colgante en su transmisión de fuerzas de tensión, con un pilar anterior que se extiende desde la región anterior del SE hasta el 40% del IE; de esta manera, el manguito sigue trabajando a pesar de las roturas que aparecen con la edad en la zona crescent (Figura 1).
No todo es tendón: la importancia de la cápsula; Nimura et al.(7) (2012)
Históricamente, la cirugía del manguito ha mirado hacia la reparación de la inserción del tendón. Sin embargo, en la última década el interés en el estudio de la cápsula y el papel que juega en la biomecánica del hombro se ha disparado y hoy en día se entienden como 2 estructuras complementarias y necesarias que forman el complejo capsulotendinoso(8). Si bien la cápsula anteroinferior es bien conocida por su papel en la inestabilidad glenohumeral(9), la cápsula posterosuperior ha sido obviada mucho tiempo. Actualmente, se acepta que la cápsula superior juega un papel biomecánico fundamental en la estabilidad glenohumeral, ya que esta actúa como fulcro y previene el escape superior del húmero(10). La importancia actual de la cápsula es tal que, en el caso de las roturas masivas no reparables del manguito, se han desarrollado técnicas de reconstrucción capsular superior (RCS) con diferentes tipos de injerto y resultados iniciales interesantes, aunque su papel a largo plazo está aún por demostrar(11,12).
Nimura et al. realizan un bonito trabajo de anatomía titulado “The superior capsule of the shoulder joint complements the insertion of the rotator cuff”. Tras diseccionar la capa formada únicamente por la cápsula aislándola del resto del manguito, encuentran que, sorprendentemente, la cápsula posterosuperior representa un porcentaje de la huella mayor del esperado y, además, su grosor no es uniforme: mientras que ocupa casi todo el ancho de la inserción en la zona más inferior del IE (> 60%), presenta un espesor mínimo de aproximadamente el 20% a una distancia de 11 mm del margen anterior de la tuberosidad mayor; es precisamente en esta región de mínimo espesor capsular donde comienzan la mayoría de las RPMR; por tanto, esta zona de debilidad parece jugar un papel importante en la etiología de las roturas del manguito.
Clasificación de las roturas: Ellman et al. (1990)(13)
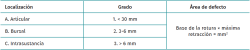
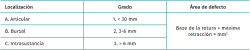
En 1990, Ellman publica esta revisión narrativa de las RPMR. Aunque ya desactualizada, resulta históricamente interesante conocer el papel que jugaron en los inicios de la cirugía del manguito técnicas diagnósticas como la artrografía, así como tratamientos actualmente menos utilizados como la reparación abierta. En su revisión, Ellman ordena las RPMR según su localización y extensión en el espesor del tendón, considerando 12 mm el 100%, dando lugar una clasificación basada en los hallazgos artroscópicos que continúa vigente y es la más utilizada (Tabla 1). Posteriormente, Snyder desarrolló otra clasificación basada en los hallazgos artroscópicos, aunque resulta más compleja, por lo que es menos utilizada(14).
Prevalencia radiológica de las roturas: Sher et al. (1995)(1)
En 1995 Jerry Sher y su equipo reclutaron 96 voluntarios sanos, sin antecedentes de síntomas en hombro o cuello, a los que hicieron una resonancia magnética (RM) que fue estudiada por 2 radiólogos expertos buscando posibles roturas del manguito; además, incluyeron como controles las RM a 20 hombros patológicos a los que realizaron una artroscopia con un 100% de diagnóstico correcto en el informe de los radiólogos. Los resultados los publicaron en el trabajo “Abnormal findings on magnetic resonance images of asymptomatic shoulders”.
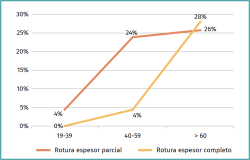
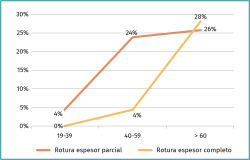
Este trabajo es muy interesante porque, con una buena metodología, nos da información de la prevalencia esperada de lesiones asintomáticas en el manguito y su relación con la edad: si bien por debajo de 40 años, las roturas parciales o totales son casi del 0%, en la franja 40-59 años encontramos un 24% de RPMR y un 4% de roturas totales, que en mayores de 60 años pasan a suponer un 26% de RPMR y hasta un 28% de RECMR. En resumen, este trabajo nos enseña que el manguito empieza a degenerarse entre los 40 y los 60 años, y que hay que ser precavidos a la hora de correlacionar la clínica con los hallazgos radiológicos, ya que casi un 60% de los mayores de 60 años que nunca han tenido síntomas presentan lesiones degenerativas en diferente grado (Figura 2).
Historia natural del manguito; Keener et al. (2015)(15)
Mientras que Sher nos daba una información de prevalencia mediante un estudio transversal de las lesiones asintomáticas del manguito, Keener et al., en su trabajo longitudinal prospectivo “A prospective evaluation of survivorship of asymptomatic degenerative rotator cuff tears”, nos explican cómo evolucionan estos hombros asintomáticos mediante un seguimiento anual clínico y ecográfico de 118 pacientes divididos en 3 grupos: pacientes con rotura parcial, pacientes con rotura total y controles sanos.
Como conclusión más relevante, los autores encontraron que el principal factor de riesgo de progresión de la lesión es el mayor grado de rotura inicial: mientras que solo el 14% de los controles presentó algún tipo de rotura, en el 44% de las RPMR y el 60% de las RECMR progresaron al menos 5 mm de manera significativa; además, la aparición de dolor se relacionó con que existiera esta progresión de la rotura. También encontraron que los pacientes con roturas más grandes al final del seguimiento habían debutado con síntomas en mayor porcentaje, aunque un 28% de los pacientes sin roturas también presentaron síntomas.
De este trabajo resultan también interesantes las curvas de supervivencia, ya que explican no solo el bajo riesgo de progresión de las RPMR, sino que cuando la rotura progresa tarda 3,3 años de media; esta información nos permite saber que estamos en un proceso degenerativo lento y nos permite estudiar a nuestros pacientes y valorar sin urgencia las opciones de tratamiento. Este mismo grupo publicó en 2023 sus datos analizando durante un tiempo de seguimiento mediano de 7,1 años la evolución de las roturas asintomáticas en población joven (< 65 años). En este grupo de población específico obtuvieron resultados similares, con una supervivencia libre de progresión del 73% a los 5 años y un tiempo mediano de 4,9 años, por lo que en pacientes jóvenes en edad laboral también disponemos de tiempo para hacer una adecuada valoración y establecer un plan de seguimiento(16).
Combinando la información que nos ofrecen los 2 últimos trabajos citados podemos concluir que la prevalencia de las lesiones en el manguito es alta, especialmente en mayores de 60 años, y no siempre deben ser consideradas patológicas. Sin embargo, en lesiones avanzadas en las que aparece dolor debemos estar alerta, porque la rotura puede estar progresando, aunque la mayoría requerirán varios años para progresar.
Controversias del tratamiento quirúrgico: cuándo operar. Kim et al. (2018)(17)
Una de las principales controversias en las RPMR es el manejo más adecuado, ya que apenas existe literatura de calidad al respecto. Actualmente, la mayoría de los cirujanos recomiendan un manejo conservador inicial de al menos 3-6 meses basado en la disociación clínico-radiológica, la baja probabilidad de progresión y, en los casos en los que progresa, el tiempo que necesita para hacerlo(18). El objetivo del tratamiento conservador es mantener un hombro funcional sin dolor o con un dolor tolerable, ya que sí se sabe que el tendón no tiene capacidad de repararse de manera espontánea sin cirugía(19). Sin embargo, en ocasiones este objetivo no se alcanza y se plantea la posibilidad de cirugía.
Ante la preocupación de algunos cirujanos de que la rotura parcial progrese rápidamente hasta perder la ventana de oportunidad de reparación, los autores de este ensayo clínico titulado “When Should We Repair Partial-Thickness Rotator Cuff Tears? Outcome Comparison Between Immediate Surgical Repair Versus Delayed Repair After 6-Month Period of Nonsurgical Treatment” comparan los resultados del tratamiento quirúrgico inmediato vs. el tratamiento quirúrgico diferido tras 6 meses de tratamiento conservador en pacientes que llevaban menos de 3 meses de síntomas. Los autores encontraron que, a los 6 meses de la cirugía, los pacientes que habían recibido tratamiento conservador prequirúrgico presentaban mejores resultados clínicos, aunque a 12 y 24 meses de seguimiento posquirúrgico los resultados clínicos se igualaban y presentaban la misma tasa de cicatrización en la RM de control. Además, de los 44 pacientes en la rama de tratamiento diferido, 10 salieron del estudio de manera voluntaria por mejoría de los síntomas. Por tanto, parece muy razonable ofrecer al menos 6 meses de tratamiento conservador en las RPMR sintomáticas, ya que existe posibilidad de mejoría sin comprometer los resultados de una potencial cirugía.
Este tipo de trabajos prospectivos aleatorizados aportan información de calidad para poder realizar recomendaciones terapéuticas, aunque son necesarios trabajos metodológicamente buenos que definan adecuadamente las diferentes opciones de tratamiento conservador y sus resultados a largo plazo.
Reparación vs. conversión: Shin (2012)(20)
Como hemos dicho, resulta comúnmente aceptado ofrecer la reparación quirúrgica en pacientes sintomáticos tras un periodo de al menos 6 meses de tratamiento conservador y más del 50% de afectación del espesor(2). Las 2 técnicas más habituales en las roturas articulares son la reparación transtendinosa in situ (realizar un desbridamiento del tendón roto y una sutura en la que haya contacto entre este y el hueso, manteniendo el remanente en continuidad con la huella) y la conversión y reparación (completar la rotura y realizar una sutura como en las RECMR); si bien completar la rotura asegura la retirada del tejido degenerado y realizar la sutura con tejido viable, el sacrificio del remanente genera preocupación por la cicatrización, al generar una rotura completa.
En este trabajo, titulado “A Comparison of 2 Repair Techniques for Partial-Thickness Articular-Sided Rotator Cuff Tears”, Shin aleatoriza 48 pacientes a recibir una u otra técnica de reparación y los sigue durante 2 años. Clínicamente, aunque a 3 meses los pacientes están clínicamente mejor con la conversión y reparación, los resultados son equivalentes en el resto del seguimiento. En el grupo de reparación se observó una mayor tasa de rerrotura (0 vs. 8%), aunque no empeoró los resultados de los pacientes. Otros estudios realizados posteriormente tampoco encontraron diferencias entre las 2 técnicas, por lo que actualmente no se puede recomendar una sobre otra(21,22).
Conclusiones
A través de estos trabajos se define la histología y la anatomía macroscópica del manguito posterosuperior. En la biomecánica y la patología de las roturas parciales es fundamental entender que existe una zona de debilidad en el límite posterior del SE y cómo trabaja el engrosamiento capsular del “cable rotador” para transmitir la fuerza cuando se inicia la rotura.
La aparición de RPMR se inicia en la 5.ª década de la vida, aumentan con la edad, aunque requieren varios años para progresar.
La primera opción terapéutica en las RPMR es el tratamiento conservador durante al menos 6 meses, aunque en la literatura aún no está definido el mejor protocolo conservador.
En los casos en los que sea necesario el tratamiento quirúrgico, los resultados de la reparación in situ vs. conversión y reparación son equivalentes, por lo que el cirujano debe decidir la mejor estrategia según el caso y su experiencia.
Figuras
Figura 1. Esquema del funcionamiento del sistema de suspensión del cable rotador. * Zona crescent; CR: cable rotador; TM: trocánter mayor; Tm: trocánter menor.
Tablas
Información del artículo
Cita bibliográfica
Autores
Beatriz Garcia Maya
Hospital Universitario Infanta Elena. Valdemoro, Madrid
Responsabilidades éticas
Conflicto de interés. Los autores declaran no tener ningún conflicto de interés.
Financiación. Este trabajo no ha sido financiado.
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Referencias bibliográficas
-
1Sher JS, Uribe JW, Posada A, Murphy BJ, Zlatkin MB. Abnormal findings on magnetic resonance images of asymptomatic shoulders. J Bone Joint Surg Am. 1995;77(1):10-5.
-
2Plancher KD, Shanmugam J, Briggs K, Petterson SC. Diagnosis and Management of Partial Thickness Rotator Cuff Tears: A Comprehensive Review. J Am Acad Orthop Surg. 2021 Dec 15;29(24):1031-43.
-
3Clark JM, Harryman DT. Tendons, ligaments, and capsule of the rotator cuff. Gross and microscopic anatomy. J Bone Joint Surg Am. 1992;74(5):713-25.
-
4Burkhart SS, Esch JC, Jolson RS. The rotator crescent and rotator cable: an anatomic description of the shoulder's "suspension bridge". Arthroscopy. 1993;9(6):611-6.
-
5Codman EA, Akerson IB. The pathology associated with rupture of the supraespinatus tendon. Ann Surg. 1931;93(1):348-59.
-
6Burkhart SS. Fluoroscopic comparison of kinematic patterns in massive rotator cuff tears. A suspension bridge model. Clin Orthop Relat Res. 1992;(284):144-52.
-
7Nimura A, Kato A, Yamaguchi K, et al. The superior capsule of the shoulder joint complements the insertion of the rotator cuff. J Shoulder Elbow Surg. 2012 Jul;21(7):867-72.
-
8Adams CR, DeMartino AM, Rego G, Denard PJ, Burkhart SS. The Rotator Cuff and the Superior Capsule: Why We Need Both. Arthroscopy. 2016 Dec;32(12):2628-37.
-
9Ovesen J, Nielsen S. Stability of the shoulder joint: Cadaver study of stabilizing structures. Acta Orthop Scand. 1985;56(2):149-51.
-
10Ishihara Y, Mihata T, Tamboli M, et al. Role of the superior shoulder capsule in passive stability of the glenohumeral joint. J Shoulder Elbow Surg. 2014;23(5):642-8.
-
11Burkhart SS, Hartzler RU. Superior Capsular Reconstruction Reverses Profound Pseudoparalysis in Patients With Irreparable Rotator Cuff Tears and Minimal or No Glenohumeral Arthritis. Arthroscopy. 2019;35(1):22-8.
-
12Mihata T, Lee TQ, Hasegawa A, et al. Arthroscopic Superior Capsule Reconstruction Can Eliminate Pseudoparalysis in Patients With Irreparable Rotator Cuff Tears. Am J Sports Med. 2018;46(11):2707-16.
-
13Ellman H. Diagnosis and treatment of incomplete rotator cuff tears. Clin Orthop Relat Res. 1990;(254):64-74.
-
14Snyder SJ, Pachelli AF, Del Pizzo W, Friedman MJ, Ferkel RD, Pattee G. Partial thickness rotator cuff tears: Results of arthroscopic treatment. Arthroscopy. 1991;7(1):1-7.
-
15Keener JD, Galatz LM, Teefey SA, et al. A prospective evaluation of survivorship of asymptomatic degenerative rotator cuff tears. J Bone Joint Surg Am. 2015 Jan 21;97(2):89-98.
-
16Torchia MT, Sefko JA, Steger-May K, Teefey SA, Middleton WD, Keener JD. Evaluation of survivorship of asymptomatic degenerative rotator cuff tears in patients 65 years and younger: a prospective analysis with long-term follow-up. J Shoulder Elbow Surg. 2023;32(7):1432-44.
-
17Kim YS, Lee HJ, Kim JH, Noh DY. When Should We Repair Partial-Thickness Rotator Cuff Tears? Outcome Comparison Between Immediate Surgical Repair Versus Delayed Repair After 6-Month Period of Nonsurgical Treatment. Am J Sports Med. 2018 Apr;46(5):1091-6.
-
18Matthewson G, Beach CJ, Nelson AA, et al. Partial Thickness Rotator Cuff Tears: Current Concepts. Adv Orthop. 2015;2015:458786.
-
19Sugaya H, Maeda K, Matsuki K, Moriishi J. Functional and structural outcome after arthroscopic full-thickness rotator cuff repair: Single-row versus dual-row fixation. Arthroscopy. 2005;21(11):1307-16.
-
20Shin SJ. A Comparison of 2 Repair Techniques for Partial-Thickness Articular-Sided Rotator Cuff Tears. Arthroscopy. 2012;28(1):25-33.
-
21Castagna A, Borroni M, Garofalo R, et al. Deep partial rotator cuff tear: transtendon repair or tear completion and repair? A randomized clinical trial. Knee Surg Sports Traumatol Arthrosc. 2015 Feb;23(2):460-3.
-
22Castricini R, La Camera F, De Gori M, et al. Functional outcomes and repair integrity after arthroscopic repair of partial articular supraspinatus tendon avulsion. Arch Orthop Trauma Surg. 2019;139(3):369-75.
Descargar artículo:
Licencia:
Este contenido es de acceso abierto (Open-Access) y se ha distribuido bajo los términos de la licencia Creative Commons CC BY-NC-ND (Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional) que permite usar, distribuir y reproducir en cualquier medio siempre que se citen a los autores y no se utilice para fines comerciales ni para hacer obras derivadas.
Comparte este contenido
En esta edición
- Desde el inicio hasta la cima: la historia de las osteotomías de rodilla
- Resultados clínico-funcionales y radiográficos de la osteotomía tibial de apertura medial valguizante
- Tendinopatía rotuliana: una guía práctica de consenso para la elección del mejor tratamiento
- Evolución de la endoscopia de columna. ¿De dónde venimos y a dónde vamos?
- Roturas parciales del manguito rotador
- Descompresión central de la cabeza femoral artroscópica más colocación de células madre autólogas como tratamiento de la osteonecrosis de la cabeza femoral
- Plastia extraarticular como gesto único en la corrección de la inestabilidad rotacional por rotura del ligamento cruzado anterior en un paciente de edad avanzada
- Osteosíntesis completamente artroscópica con botón de fractura aguda de glenoides anterior: reporte de caso
- Visualización artroscópica del hiato poplíteo y localización de un cuerpo libre intraarticular
Más en PUBMED
Más en Google Scholar
Más en ORCID


Revista Española de Artroscopia y Cirugía Articular está distribuida bajo una licencia de Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional.