Infección aguda en fractura tratada con osteosíntesis
Acute infection in fracture treated with osteosynthesis
Resumen:
El tratamiento de la complicación infecciosa de una fractura tratada con osteosíntesis supone un gran reto. Implica dar solución a la fractura y a la vez a la infección. Y contamos con la presencia de un material externo al cuerpo que a veces lo podemos considerar como un aliado pero otras veces supone un impedimento a la curación. Son muchos los factores que intervendrán en este proceso y que deberán ser considerados al proceder al tratamiento. Este tratamiento será invariablemente quirúrgico, aunque apoyado siempre con tratamiento médico antimicrobiano.
Abstract:
The treatment of the infectious complication of fracture treated with osteosynthesis is a great challenge. It means to give solution to fracture and at the same time the infection. And counted with the presence of a foreign body material that sometimes we can consider it as an ally but sometimes represents an impediment to healing. There are many factors that intervene in this process and which should be considered when the treatment. This treatment will be invariably surgical but always supported with anti-microbial treatment.
Introducción
La presencia de una infección destaca entre todas las complicaciones posibles de una osteosíntesis. La infección añade a las posibles secuelas propias del traumatismo sobre el hueso y las partes blandas la agresión propia de un proceso séptico. Pone en riesgo el tratamiento realizado sobre la fractura, pudiendo derivar finalmente a secuelas graves o muy graves tras múltiples intervenciones y procedimientos(1).
La indicación del tratamiento dependerá de diversos factores que deben ser valorados en todo su conjunto para una actuación eficaz.
Cada factor tiene un efecto limitado, siendo la suma de todos ellos la que nos guiará hacia el tratamiento a seguir.
1. Tiempo transcurrido desde la intervención
Consideraremos como infección aguda aquella acaecida antes de las 2 semanas de la intervención. Se trata por definición de una fractura no consolidada.
La infección subaguda será aquella que aparece entre la 2.ª y la 10.ª semana de la intervención. En las subagudas iniciales la fractura no está consolidada, pero sí podría haberse iniciado la consolidación hacia el final de este periodo(2,3).
2. El grado de consolidación ósea
Este factor va relacionado con el del tiempo transcurrido desde la intervención. El estudio clínico y radiológico simple o por tomografía axial computarizada (TAC) nos permite determinar con precisión si la fractura está o no consolidada y si es permisible la extracción del implante(1,3).
3. El implante y sus características
- Material del implante: el titanio presenta en estudios experimentales una biocompatibilidad (tolerancia) superior al acero que, si bien en circunstancias de normalidad es poco significativa, en caso de infección su comportamiento variará de forma manifiesta. La adhesión de los tejidos blandos con el material de osteosíntesis evitará el espacio muerto entre ambos. Con ello se evita que las bacterias crezcan y se reproduzcan en este espacio(4).
- Diseño del implante: las placas de bajo contacto (low contact dynamic compression plate –LC-DCP–) elevan la superficie de aproximación implante-hueso, disminuyendo la zona de apoyo. Ello favorece la preservación de la vascularización perióstica, evitando la necrosis por contacto. En su superficie externa, el diseño de la placa debe favorecer el deslizamiento de las partes blandas, disminuyendo la fricción mecánica y evitando tejido fibroso poco vascularizado(4). En los clavos endomedulares, los clavos sólidos presentan en estudios menor índice de infección que los ranurados debido a que los espacios muertos existentes en las ranuras y dentro del clavo permiten la propagación de bacterias(5).
- Alergenicidad: el acero inoxidable presenta un 10% de níquel, que es un alérgeno conocido. Un 25% de las mujeres presenta alergia por contacto con el níquel. Este dato puede ser de relevancia como factor predisponente a una infección o en el diagnóstico diferencial(4).
- Tipo de implante: placa versus clavo. La actuación quirúrgica sobre una osteosíntesis infectada de placa atornillada diferirá significativamente respecto a la de un clavo endomedular. En el primer caso tenemos la posibilidad de mantener el implante; en cambio, en el caso del enclavado endomedular la infección se extiende por el canal endomedular, por lo que debemos remover el implante para proceder al desbridamiento endomedular.
4. Características de la fractura
Ante una fractura articular, el objetivo es mantener el implante, que nos garantiza la preservación de la interlínea articular. En cambio, una fractura extraarticular puede permitir la extracción o el reemplazo del implante si ello fuera necesario.
La localización de la infección y la protección ósea por las partes blandas es un factor determinante en la decisión del tratamiento de una síntesis infectada. El respeto a la biología en cuanto a la vía de acceso y las maniobras quirúrgicas realizadas en la primera intervención para la implantación de una osteosíntesis son primordiales para valorar el estado de los tejidos blandos y pueden modificar la resistencia a la infección. El estado de las partes blandas es vital para la llegada de un buen flujo sanguíneo a la zona de la lesión que facilite la curación, la resistencia a la infección y la llegada del tratamiento antibiótico. Un buen trofismo de las partes blandas facilitará la permanencia del implante, pero ante una gran atricción y baja viabilidad de los tejidos tendemos habitualmente a la retirada del implante(6).
5. Según la estabilidad de la osteosíntesis
La estabilidad mecánica es esencial para la consolidación de una fractura. Una fractura con una osteosíntesis estable curará, a pesar de la infección. Por el contrario, la pérdida de estabilidad que comporta el proceso séptico sobre la osteosíntesis puede llevar a la no curación de la fractura, por lo que a la infección añadimos el problema del retardo de la consolidación o una pseudoartrosis infectada(2,4,6).
La infección es por ella misma causa de aflojamiento de los implantes, especialmente de los tornillos, aunque estos implantes hubieran sido estables en el momento del diagnóstico inicial de la infección6). Los micromovimientos en una osteosíntesis inestable, la necrosis por contacto, por la misma infección ósea y la producida por el mismo brocado o fresado óseo provocan pérdida por reabsorción ósea con aflojamiento de los implantes intensificando la presencia de infección. La reestabilización de la fractura favorecerá la curación ósea. Los secuestros óseos que impiden la consolidación y mantienen la infección deben ser extirpados en su totalidad.
Existen datos clínicos preoperatorios que sugieren inestabilidad y que debemos tener en cuenta: la presencia de lisis alrededor de los tornillos en la radiología simple, la movilidad del foco de fractura a pesar de la presencia de la osteosíntesis y la movilización secundaria de los implantes respecto a su situación original.
6. El germen
La agresividad del germen será un factor determinante. Un germen poco agresivo nos permitirá con mayor facilidad mantener el implante. En cambio, un germen muy resistente compromete la permanencia del implante. Hemos de tener en cuenta que un porcentaje de las infecciones pueden ser nosocomiales, con gérmenes multirresistentes, lo que dificulta el manejo terapéutico(2,6).
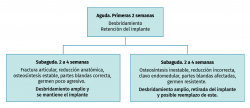
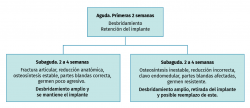
En la Figura 1 se presenta un algoritmo de actuación práctica ante una osteosíntesis infectada.
Tratamiento
El tratamiento se basa en la práctica de un desbridamiento precoz de la región afectada asociada a un tratamiento antibiótico prolongado(6,7).
Ante el diagnóstico de sospecha de infección de una osteosíntesis el desbridamiento debe ser inmediato y agresivo. A mayor precocidad de la actuación quirúrgica, mayor posibilidad de curación. También la calidad del desbridamiento influye en los resultados finales, habiendo mayores posibilidades de curación tras la práctica de una adecuada limpieza quirúrgica(8). El desbridamiento debe ser amplio, suficiente para actuar sobre toda la superficie afectada. Conviene recordar que un implante infectado lo será en su totalidad y no parcialmente(3).
A la actuación quirúrgica le seguirá un tratamiento antibiótico inicialmente intravenoso y de amplio espectro en espera de conocer el germen responsable. Si los cultivos permiten identificar al germen, se cambiará a antibioticoterapia específica(6).
Actuación ante una infección aguda de una fractura tratada con osteosíntesis
1. Obtención de muestras: la primera actuación estará encaminada a obtener muestras de material biológico para el cultivo bacteriológico. Debemos dotar al microbiólogo de muestras de calidad para facilitar su trabajo. La identificación inequívoca del germen responsable del proceso séptico permitirá la aplicación del tratamiento antibiótico específico según su sensibilidad. Las muestras a extraer deben ser en número y calidad suficiente para aumentar las posibilidades de positivización. Normalmente se toman un mínimo de 3, aunque es preferible la toma de 5 o 6 muestras(9). Estas se extraen de localizaciones distintas. Es recomendable cultivar muestras de tejidos y de hueso, dado que en ellas podremos encontrar bacterias sésiles. Las muestras líquidas suelen dar menos información, dado que en ellas solo encontramos las bacterias libres o planctónicas, no así las bacterias sésiles, adheridas al biofilm(10). El rendimiento de las muestras líquidas aumenta si se cultivan en frascos de hemocultivo(9). Se puede remitir el implante para cultivo y, por técnica de sonicación (uso de ultrasonidos para despegar el biofilm del implante), poder estudiar los gérmenes adheridos a él. Este proceso de extracción de muestra del implante presenta un riesgo de contaminación elevado, por lo que los resultados pueden verse falseados y dar lugar a dificultades en su interpretación(2,9,10).
La existencia de un tratamiento antibiótico previo a la toma de muestras puede alterar los resultados obtenidos. Es por ello que se debe evitar el tratamiento antibiótico empírico antes de obtener las muestras quirúrgicas.
2. Desbridamiento y escisión del tejido necrosado: el desbridamiento se basa en la resección quirúrgica de todo el tejido no viable o de baja viabilidad, secuestros óseos, esfacelos, fibrina. La capacidad de sangrado de los tejidos nos aporta información de su viabilidad. Un suministro suficiente de sangre a los tejidos es un requisito imprescindible para la curación y la resistencia a la infección. Limpiamos las superficies metálicas del implante en osteosíntesis con placa atornillada. Se recomienda realizar la limpieza sin pensar en la reconstrucción futura, tema a considerar cuando proceda(1,4,6,7).
3. Irrigación: tras el desbridamiento quirúrgico se procede al lavado con abundante suero salino pulsado a baja presión(1). El uso de flujo de suero a alta presión puede favorecer la inoculación del germen en los tejidos adyacentes, extendiendo la infección. Un buen lavado disminuye significativamente el recuento bacteriano, clave para el control de la infección(3).
4. Comprobación de la estabilidad de la fijación y los implantes: el objetivo es preservar la osteosíntesis en la fase precoz del tratamiento de la fractura(3), por lo que los implantes que mantengan la estabilidad mecánica deben conservarse(5,6). En ocasiones puede requerir optimizar la osteosíntesis retirando tornillos aflojados y añadiendo otros a la osteosíntesis previa. Los criterios quirúrgicos de la nueva osteosíntesis serán los mismos que en una fractura no consolidada, o sea, proporcionar estabilidad a la fractura para lograr su curación a pesar del entorno séptico, que ya es tratado con el desbridamiento quirúrgico y con la antibioticoterapia posterior(2,3).
En el caso de las fracturas articulares, la preservación del implante cobra una mayor importancia, dado que es el garante de la congruencia articular. Mantenemos en este caso el implante en lo posible.
El tratamiento del enclavado endomedular con infección adyacente varía respecto al de la placa atornillada. Debe extraerse el clavo, fresar el canal endomedular, limpiar el canal con suero salino abundante y proceder a un nuevo enclavado de la extremidad(7,11). Si se conoce el germen responsable previamente a la intervención, es posible revestir la superficie del clavo endomedular con un antibiótico al que el germen presente sensibilidad(12).
Pasadas las semanas y una vez instalado el biofilm en los implantes, el reemplazo por otros implantes debe ser considerado para la resolución de la infección en fracturas no consolidadas.
Cuando la fractura no permita mantener el implante, sea por inestabilidad severa de la osteosíntesis, mala calidad ósea, pérdida ósea significativa o por el fracaso de las partes blandas, procedemos a la retirada completa del material de osteosíntesis y a valorar la colocación de un fijador externo, que nos proporciona la estabilidad eficaz de la fractura y nos permite tratar las partes blandas(3,6). La estabilidad de un fijador externo es menor que la que nos ofrece un sistema de fijación interna, por lo que se suele recomendar reconvertir la fijación externa en una fijación interna en cuanto ello sea posible, dada la mayor tasa de pseudoartrosis que presenta el tratamiento con fijación externa respecto a la fijación interna.
Se puede asociar a los implantes cemento con antibiótico incluido. Puede rellenar defectos óseos o reforzar la estructura ósea. La proporción de antibiótico a incluir al cemento debe ser de 1 a 10. Aumentar esta proporción compromete las propiedades mecánicas del cemento. Se han usado asociaciones de cemento con vancomicina, gentamicina, tobramicina y ciprofloxacino. El antibiótico suele liberarse entre 2-6 semanas, perdiendo posteriormente la capacidad antibiótica. Se ha descrito la aparición de una membrana que se forma alrededor del cemento. Si esta membrana se preserva, puede ser aprovechada para envolver los tejidos o para alojar injerto óseo si fuera preciso en una nueva cirugía. La membrana aumenta la capacidad osteoinductora, ayudando a la curación de la fractura y, por consiguiente, de la infección(1,13).
En infecciones tardías de 6 a 10 semanas en las que objetivamos la consolidación de la fractura, se puede retirar el material de osteosíntesis implantado y tratar la osteítis residual, con desbridamiento de secuestros óseos y valorando la posibilidad de aporte de injerto óseo autólogo(7).
5. Cierre primario de la herida quirúrgica: intentamos el cierre de la herida quirúrgica si es posible, dado que nos protege la fractura del exterior evitando una sobreinfección. Si no fuera posible, se puede conseguir la cobertura cutánea de los tejidos blandos y el aporte sanguíneo adecuado mediante injertos y colgajos.
El uso de apósitos con sistemas de presión negativa se ha relacionado con la disminución del porcentaje de infecciones y de necrosis de los tejidos. El mecanismo de succión elimina los espacios muertos y promueve el contacto de la misma manera que lo realiza un vendaje a compresión(4,11).
6. Instauración de tratamiento antibiótico intravenoso de amplio espectro. Su inicio será inmediato tras la finalización del desbridamiento quirúrgico. No debe iniciarse antes de proceder a la actuación quirúrgica. La existencia de un tratamiento antibiótico previo a la toma de las muestras puede alterar los resultados obtenidos.
La antibioticoterapia de amplio espectro se mantiene mientras no se tenga una identificación positiva del germen responsable de la infección y su sensibilidad a los diferentes antibióticos(7).
En algunos casos con comorbilidad múltiple o con gran exigencia en el tratamiento, puede valorarse la opción conservadora, con antibioticoterapia supresiva a largo plazo y evitando la solicitación de la osteosíntesis(2).
Información del artículo
Cita bibliográfica
Autores
Jordi Bertrán Padrós
Cirugía Ortopédica y Traumatología. Hospital de Barcelona
Unión de Mutuas. Barcelona
Jose Miguel Sales Pérez
Complex Hospitalari Moisès Broggi. Sant Joan Despí, Barcelona
Servicio de Cirugia Ortopédica y Traumatología, Consorci Sanitari Integral, Barcelona, España
Unión de Mutuas. Barcelona
Responsabilidades éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Financiación. Los autores declaran que este trabajo no ha sido financiado.
Conflicto de interés. Los autores declaran no tener ningún conflicto de intereses.
Referencias bibliográficas
-
1Mazurek MT, Girard PJ. Capítulo 3. Infecciones. En: Horwitz DS, Cordero Ampuero J (coords.). Infecciones. Monografías AAOS- SECOT; 2012. pp. 31-42.
-
2Trampuz A, Widmer AF. Infections associated with orthopedic implants. Curr Opin Infect Dis. 2006 Aug;19(4):349-56.
-
3Jenny JY, Gaudias J. Principios del tratamiento de la infección ósea. EMC-Técnicas quirúrgicas en ortopedia y traumatología. 2013 Dic;5(4).
-
4Perren SM, Fernández Dell’Oca A, Regazzoni P. Infection after internal fixation. Part 2: Biology. ICUC Paper; 2017.
-
5Perren SM, Fernández Dell’Oca A, Regazzoni P. Infection after internal fixation. Part 1: Biomechanics. ICUC Paper; 2017.
-
6Rüedi T. Tratamiento de la infección aguda tras el tratamiento quirúrgico de las fracturas. AO International.
-
7Tenaglia K, Medina J. Osteomielitis de huesos largos asociada a osteosíntesis y actualización de las infecciones de prótesis articulares. Cátedra de Enfermedades Infecciosas; 2017.
-
8Enninghorst N, McDougall D, Joshua RN, Hunt J, Balogh ZJ. Open Tibia Fractures: timely debridement leaves injury severity as the only determinant of poor outcome. J Trauma. 2011 Feb;70(2):352-6; discussion 356-7.
-
9Sánchez Romero I, del Pozo JL, Villanueva M. Infección osteoarticular. Abordaje desde una perspectiva multidiciplinar. Infección y vacunas; 2013.
-
10Cordero Ampuero J, Esteban J. Capítulo 4. Nuevas posibilidades en el diagnóstico de la infección osteoarticular. En: Horwitz DS, Cordero Ampuero J (coords.). Infecciones. Monografías AAOS- SECOT; 2012. pp. 43-50.
-
11Palomino J, Puente A, López M, Valencia J, Aguilera C, López Cortés, Jiménez M. Osteomielitis de huesos largos e infección asociada a material de osteosíntesis. Guía PRIOAM; 2017.
-
12Raghuram T, Conway J. Antibiotic cement-coated interlocking nail for the treatment of infected nonunions and segmental bone defects. J Orthop Trauma. 2007 Apr;21(4):258-68.
-
13Pelissier P, Masquelet AC, Bareille R, Pelissier S, Amadee J. Induced membranes secrete growth factors including vascular and osteoinductive factors and could stimulate bone regeneration. J Orthop Res. 2004 Jan;22(1):73-9.
Descargar artículo:
Licencia:
Este contenido es de acceso abierto (Open-Access) y se ha distribuido bajo los términos de la licencia Creative Commons CC BY-NC-ND (Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional) que permite usar, distribuir y reproducir en cualquier medio siempre que se citen a los autores y no se utilice para fines comerciales ni para hacer obras derivadas.
Comparte este contenido
En esta edición
- Juntos, avanzamos y crecemos
- Seguimos adelante
- La infección asociada a la asistencia sanitaria en el entorno laboral
- Infección aguda en fractura tratada con osteosíntesis
- Artritis séptica de rodilla tras artroscopia de reconstrucción de ligamento cruzado anterior
- Pseudoartrosis séptica. Actualización en manejo y tratamiento
- Osteítis crónica
- Clínica Online: una herramienta útil para profesionales sanitarios y pacientes en medicina laboral
- Terapia de presión negativa con instilación en pacientes traumatológicos
- Propuesta de un protocolo de abordaje fisioterapéutico en pacientes en situación de baja laboral pendientes de intervención quirúrgica
- Análisis de la eficacia sobre el dolor y la capacidad funcional en el abordaje terapéutico de la epicondilopatía lateral crónica del codo con ondas de choque extracorpóreas radiales
- Plastia de rotación del ancóneo: una opción de rescate tras cirugía en epicondilitis crónica rebelde al tratamiento
- Accidente por electrización. ¡Estoy vivo!
Más en PUBMED
Más en Google Scholar


Revista Española de Traumatología Laboral está distribuida bajo una licencia de Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional.